Nel campo della medicina moderna, gli antibiotici si sono dimostrati uno dei progressi più significativi, riducendo drasticamente l'incidenza e la mortalità associate alle infezioni microbiche. La loro capacità di modificare l'esito clinico delle infezioni batteriche ha allungato l'aspettativa di vita di innumerevoli pazienti. Gli antibiotici sono fondamentali in procedure mediche complesse, tra cui interventi chirurgici, impianti, trapianti e chemioterapia. Tuttavia, l'emergere di patogeni resistenti agli antibiotici è diventato una preoccupazione crescente, riducendo nel tempo l'efficacia di questi farmaci. Casi di resistenza agli antibiotici sono stati documentati in tutte le categorie di antibiotici a seguito di mutazioni microbiche. La pressione selettiva esercitata dai farmaci antimicrobici ha contribuito alla diffusione di ceppi resistenti, rappresentando una sfida significativa per la salute globale.
Per contrastare l'urgente problema della resistenza antimicrobica, è fondamentale implementare politiche efficaci di controllo delle infezioni che limitino la diffusione di patogeni resistenti, riducendo al contempo l'utilizzo di antibiotici. Inoltre, vi è un'urgente necessità di metodi di trattamento alternativi. L'ossigenoterapia iperbarica (HBOT) si è affermata come una modalità promettente in questo contesto, prevedendo l'inalazione di ossigeno al 100% a specifici livelli di pressione per un determinato periodo di tempo. Proposta come trattamento primario o complementare per le infezioni, l'HBOT potrebbe offrire nuove speranze nel trattamento delle infezioni acute causate da patogeni resistenti agli antibiotici.
Questa terapia viene sempre più utilizzata come trattamento primario o alternativo per diverse patologie, tra cui infiammazioni, intossicazione da monossido di carbonio, ferite croniche, malattie ischemiche e infezioni. Le applicazioni cliniche dell'ossigenoterapia iperbarica nel trattamento delle infezioni sono notevoli e offrono vantaggi inestimabili ai pazienti.

Applicazioni cliniche dell'ossigenoterapia iperbarica nelle infezioni
Le evidenze attuali supportano in modo convincente l'applicazione dell'ossigenoterapia iperbarica (HBOT), sia come trattamento autonomo che adiuvante, apportando benefici significativi ai pazienti infetti. Durante l'HBOT, la pressione parziale di ossigeno nel sangue arterioso può raggiungere i 2000 mmHg e il conseguente elevato gradiente pressorio tissutale può innalzare i livelli di ossigeno nei tessuti fino a 500 mmHg. Tali effetti sono particolarmente utili per favorire la guarigione delle risposte infiammatorie e delle alterazioni microcircolatorie osservate in ambienti ischemici, nonché nella gestione della sindrome compartimentale.
L'HBOT può anche avere un impatto sulle condizioni che dipendono dal sistema immunitario. La ricerca indica che l'HBOT può sopprimere le sindromi autoimmuni e le risposte immunitarie indotte da antigeni, contribuendo a mantenere la tolleranza del trapianto riducendo la circolazione di linfociti e leucociti e modulando le risposte immunitarie. Inoltre, l'HBOTfavorisce la guarigionenelle lesioni cutanee croniche stimolando l'angiogenesi, un processo fondamentale per una migliore guarigione. Questa terapia favorisce inoltre la formazione della matrice di collagene, una fase essenziale nella cicatrizzazione delle ferite.
Occorre prestare particolare attenzione ad alcune infezioni, soprattutto a quelle profonde e difficili da trattare, come la fascite necrotizzante, l'osteomielite, le infezioni croniche dei tessuti molli e l'endocardite infettiva. Una delle applicazioni cliniche più comuni dell'ossigenoterapia iperbarica (HBOT) è il trattamento delle infezioni cutanee e dei tessuti molli e dell'osteomielite associate a bassi livelli di ossigeno, spesso causate da batteri anaerobi o resistenti.
1. Infezioni del piede diabetico
piede diabeticoLe ulcere sono una complicanza frequente nei pazienti diabetici, interessando fino al 25% di questa popolazione. Le infezioni insorgono spesso in queste ulcere (rappresentando il 40-80% dei casi) e comportano un aumento della morbilità e della mortalità. Le infezioni del piede diabetico (DFI) sono generalmente costituite da infezioni polimicrobiche con l'identificazione di diversi patogeni batterici anaerobi. Diversi fattori, tra cui difetti della funzione dei fibroblasti, problemi di formazione del collagene, meccanismi immunitari cellulari e funzione dei fagociti, possono ostacolare la guarigione delle ferite nei pazienti diabetici. Diversi studi hanno identificato la ridotta ossigenazione cutanea come un forte fattore di rischio per le amputazioni correlate alle DFI.
Come una delle opzioni attuali per il trattamento DFIÈ stato dimostrato che l'ossigenoterapia iperbarica (HBOT) migliora significativamente i tassi di guarigione delle ulcere del piede diabetico, riducendo di conseguenza la necessità di amputazioni e interventi chirurgici complessi. Non solo minimizza la necessità di procedure che richiedono ingenti risorse, come interventi di chirurgia a lembo e innesti cutanei, ma presenta anche costi inferiori ed effetti collaterali minimi rispetto alle opzioni chirurgiche. Uno studio di Chen et al. ha dimostrato che più di 10 sedute di HBOT hanno portato a un miglioramento del 78,3% nei tassi di guarigione delle ferite nei pazienti diabetici.
2. Infezioni necrotizzanti dei tessuti molli
Le infezioni necrotizzanti dei tessuti molli (NSTI) sono spesso polimicrobiche, in genere derivanti da una combinazione di patogeni batterici aerobici e anaerobici e sono spesso associate alla produzione di gas. Sebbene le NSTI siano relativamente rare, presentano un alto tasso di mortalità a causa della loro rapida progressione. Una diagnosi e un trattamento tempestivi e appropriati sono fondamentali per ottenere risultati favorevoli e l'HBOT è stata raccomandata come metodo aggiuntivo per la gestione delle NSTI. Sebbene permanga una controversia sull'uso dell'HBOT nelle NSTI a causa della mancanza di studi controllati prospettici,Le prove suggeriscono che potrebbe essere correlato a migliori tassi di sopravvivenza e alla conservazione degli organi nei pazienti con infezioni necrotizzanti dei tessuti molli.Uno studio retrospettivo ha indicato una significativa riduzione dei tassi di mortalità tra i pazienti con infezioni necrotizzanti dei tessuti molli (NSTI) sottoposti a terapia iperbarica (HBOT).
1.3 Infezioni del sito chirurgico
Le infezioni del sito chirurgico (SSI) possono essere classificate in base alla sede anatomica dell'infezione e possono essere causate da diversi agenti patogeni, inclusi batteri sia aerobi che anaerobi. Nonostante i progressi nelle misure di controllo delle infezioni, come le tecniche di sterilizzazione, l'uso di antibiotici profilattici e i miglioramenti nelle pratiche chirurgiche, le SSI rimangono una complicanza persistente.
Una revisione significativa ha esaminato l'efficacia dell'ossigenoterapia iperbarica (HBOT) nella prevenzione delle infezioni profonde del sito chirurgico (SSI) nella chirurgia della scoliosi neuromuscolare. L'HBOT preoperatoria può ridurre significativamente l'incidenza delle SSI e favorire la guarigione delle ferite. Questa terapia non invasiva crea un ambiente in cui i livelli di ossigeno nei tessuti della ferita sono elevati, il che è stato associato all'azione battericida ossidativa contro i patogeni. Inoltre, contrasta la riduzione dei livelli di ossigeno nel sangue che contribuisce allo sviluppo delle SSI. Oltre ad altre strategie di controllo delle infezioni, l'HBOT è stata raccomandata in particolare per interventi chirurgici pulito-contaminati come le procedure colorettali.
1.4 Ustioni
Le ustioni sono lesioni causate da calore estremo, corrente elettrica, sostanze chimiche o radiazioni e possono comportare alti tassi di morbilità e mortalità. L'ossigenoterapia iperbarica (HBOT) è utile nel trattamento delle ustioni perché aumenta i livelli di ossigeno nei tessuti danneggiati. Mentre gli studi su animali e clinici presentano risultati contrastanti riguardol'efficacia dell'HBOT nel trattamento delle ustioniUno studio condotto su 125 pazienti ustionati ha indicato che l'ossigenoterapia iperbarica (HBOT) non ha avuto un impatto significativo sui tassi di mortalità o sul numero di interventi chirurgici eseguiti, ma ha ridotto il tempo medio di guarigione (19,7 giorni rispetto a 43,8 giorni). L'integrazione dell'HBOT con una gestione completa delle ustioni potrebbe controllare efficacemente la sepsi nei pazienti ustionati, portando a tempi di guarigione più brevi e a una riduzione del fabbisogno di liquidi. Tuttavia, sono necessarie ulteriori e approfondite ricerche prospettiche per confermare il ruolo dell'HBOT nella gestione delle ustioni estese.
1.5 Osteomielite
L'osteomielite è un'infezione dell'osso o del midollo osseo, spesso causata da batteri patogeni. Il trattamento dell'osteomielite può essere complesso a causa della scarsa irrorazione sanguigna delle ossa e della limitata penetrazione degli antibiotici nel midollo. L'osteomielite cronica è caratterizzata dalla persistenza di agenti patogeni, da una lieve infiammazione e dalla formazione di tessuto osseo necrotico. L'osteomielite refrattaria si riferisce a infezioni ossee croniche che persistono o si ripresentano nonostante un trattamento adeguato.
È stato dimostrato che l'ossigenoterapia iperbarica (HBOT) migliora significativamente i livelli di ossigeno nei tessuti ossei infetti. Numerose casistiche e studi di coorte indicano che l'HBOT migliora gli esiti clinici per i pazienti affetti da osteomielite. Sembra agire attraverso diversi meccanismi, tra cui l'aumento dell'attività metabolica, la soppressione dei patogeni batterici, il potenziamento degli effetti antibiotici, la riduzione dell'infiammazione e la promozione della guarigione.processi. Dopo l'HBOT, dal 60% all'85% dei pazienti con osteomielite cronica refrattaria mostrano segni di soppressione dell'infezione.
1.6 Infezioni fungine
A livello globale, oltre tre milioni di persone soffrono di infezioni fungine croniche o invasive, che causano oltre 600.000 decessi all'anno. L'efficacia del trattamento delle infezioni fungine è spesso compromessa da fattori quali alterazioni dello stato immunitario, patologie preesistenti e caratteristiche di virulenza del patogeno. L'ossigenoterapia iperbarica (HBOT) si sta affermando come un'opzione terapeutica promettente per le infezioni fungine gravi, grazie alla sua sicurezza e alla sua natura non invasiva. Studi indicano che l'HBOT potrebbe essere efficace contro patogeni fungini come Aspergillus e Mycobacterium tuberculosis.
L'ossigenoterapia iperbarica (HBOT) promuove effetti antifungini inibendo la formazione di biofilm di Aspergillus, con una maggiore efficacia riscontrata nei ceppi privi del gene della superossido dismutasi (SOD). Le condizioni ipossiche durante le infezioni fungine rappresentano una sfida per la somministrazione di farmaci antifungini, rendendo l'aumento dei livelli di ossigeno fornito dall'HBOT un intervento potenzialmente benefico, sebbene siano necessarie ulteriori ricerche.
Le proprietà antimicrobiche dell'ossigenoterapia iperbarica
L'ambiente iperossico creato dall'ossigenoterapia iperbarica (HBOT) innesca cambiamenti fisiologici e biochimici che stimolano le proprietà antibatteriche, rendendola un'efficace terapia adiuvante per le infezioni. L'HBOT dimostra notevoli effetti contro i batteri aerobici e prevalentemente anaerobici attraverso meccanismi quali l'attività battericida diretta, il potenziamento delle risposte immunitarie e gli effetti sinergici con specifici agenti antimicrobici.
2.1 Effetti antibatterici diretti dell'ossigenoterapia iperbarica
L'effetto antibatterico diretto dell'ossigenoterapia iperbarica (HBOT) è in gran parte attribuito alla generazione di specie reattive dell'ossigeno (ROS), tra cui anioni superossido, perossido di idrogeno, radicali idrossilici e ioni idrossido, tutti prodotti durante il metabolismo cellulare.
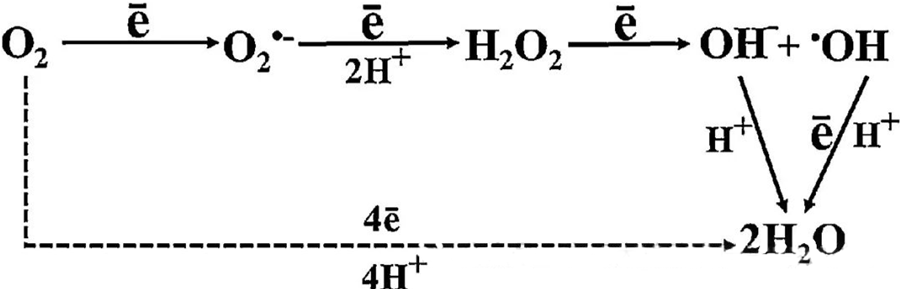
L'interazione tra O₂ e i componenti cellulari è fondamentale per comprendere come si formano le specie reattive dell'ossigeno (ROS) all'interno delle cellule. In determinate condizioni, note come stress ossidativo, l'equilibrio tra la formazione e la degradazione delle ROS viene alterato, portando a livelli elevati di ROS nelle cellule. La produzione di superossido (O₂⁻) è catalizzata dalla superossido dismutasi, che successivamente converte O₂⁻ in perossido di idrogeno (H₂O₂). Questa conversione viene ulteriormente amplificata dalla reazione di Fenton, che ossida Fe²⁺ generando radicali idrossilici (·OH) e Fe³⁺, innescando così una sequenza redox dannosa di formazione di ROS e danno cellulare.
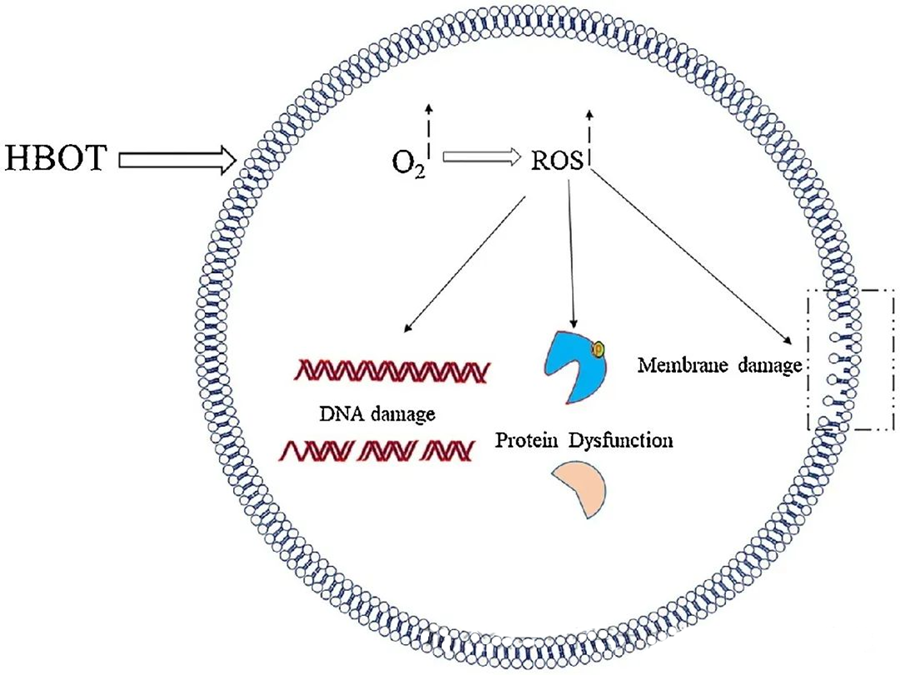
Gli effetti tossici delle specie reattive dell'ossigeno (ROS) colpiscono componenti cellulari critici come DNA, RNA, proteine e lipidi. In particolare, il DNA è un bersaglio primario della citotossicità mediata da H₂O₂, poiché altera le strutture del deossiribosio e danneggia la composizione delle basi. Il danno fisico indotto dalle ROS si estende alla struttura ad elica del DNA, potenzialmente a causa della perossidazione lipidica innescata dalle ROS stesse. Ciò sottolinea le conseguenze negative di livelli elevati di ROS all'interno dei sistemi biologici.
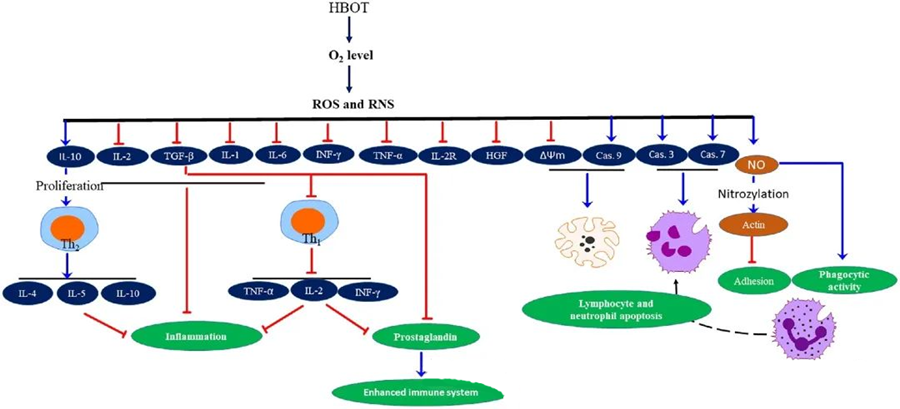
Azione antimicrobica delle ROS
Le specie reattive dell'ossigeno (ROS) svolgono un ruolo fondamentale nell'inibire la crescita microbica, come dimostrato dalla generazione di ROS indotta dall'ossigenoterapia iperbarica (HBOT). Gli effetti tossici delle ROS colpiscono direttamente i costituenti cellulari come DNA, proteine e lipidi. Elevate concentrazioni di specie reattive dell'ossigeno possono danneggiare direttamente i lipidi, causando la perossidazione lipidica. Questo processo compromette l'integrità delle membrane cellulari e, di conseguenza, la funzionalità dei recettori e delle proteine associate alla membrana.
Inoltre, le proteine, che sono anch'esse importanti bersagli molecolari delle specie reattive dell'ossigeno (ROS), subiscono specifiche modificazioni ossidative a livello di vari residui amminoacidici come cisteina, metionina, tirosina, fenilalanina e triptofano. Ad esempio, è stato dimostrato che l'ossigenoterapia iperbarica (HBOT) induce cambiamenti ossidativi in diverse proteine di E. coli, tra cui il fattore di allungamento G e DnaK, influenzandone così le funzioni cellulari.
Potenziare l'immunità attraverso l'ossigenoterapia iperbarica
Le proprietà antinfiammatorie dell'ossigenoterapia iperbaricaSono stati documentati effetti cruciali per alleviare il danno tissutale e sopprimere la progressione dell'infezione. L'ossigenoterapia iperbarica (HBOT) influenza significativamente l'espressione delle citochine e di altri regolatori infiammatori, modificando la risposta immunitaria. Diversi sistemi sperimentali hanno osservato cambiamenti differenziali nell'espressione genica e nella produzione di proteine dopo l'HBOT, che portano a una sovraregolazione o sottoregolazione dei fattori di crescita e delle citochine.
Durante il processo di ossigenoterapia iperbarica (HBOT), l'aumento dei livelli di O₂ innesca una serie di risposte cellulari, come la soppressione del rilascio di mediatori pro-infiammatori e la promozione dell'apoptosi di linfociti e neutrofili. Nel complesso, queste azioni potenziano i meccanismi antimicrobici del sistema immunitario, facilitando così la guarigione dalle infezioni.
Inoltre, studi suggeriscono che l'aumento dei livelli di O₂ durante l'ossigenoterapia iperbarica (HBOT) può ridurre l'espressione di citochine pro-infiammatorie, tra cui l'interferone-gamma (IFN-γ), l'interleuchina-1 (IL-1) e l'interleuchina-6 (IL-6). Questi cambiamenti includono anche la riduzione del rapporto tra cellule T CD4 e CD8 e la modulazione di altri recettori solubili, con conseguente aumento dei livelli di interleuchina-10 (IL-10), fondamentale per contrastare l'infiammazione e favorire la guarigione.
Le attività antimicrobiche dell'ossigenoterapia iperbarica (HBOT) sono strettamente legate a complessi meccanismi biologici. È stato riportato che sia il superossido che l'aumento della pressione promuovono, in modo non sempre coerente, l'attività antibatterica indotta dall'HBOT e l'apoptosi dei neutrofili. In seguito al trattamento con HBOT, un marcato aumento dei livelli di ossigeno potenzia le capacità battericide dei neutrofili, una componente essenziale della risposta immunitaria. Inoltre, l'HBOT sopprime l'adesione dei neutrofili, mediata dall'interazione delle β-integrine presenti sui neutrofili con le molecole di adesione intercellulare (ICAM) sulle cellule endoteliali. L'HBOT inibisce l'attività dell'integrina β-2 dei neutrofili (Mac-1, CD11b/CD18) attraverso un processo mediato dall'ossido nitrico (NO), contribuendo alla migrazione dei neutrofili verso il sito di infezione.
Il preciso riarrangiamento del citoscheletro è necessario affinché i neutrofili possano fagocitare efficacemente i patogeni. È stato dimostrato che la S-nitrosilazione dell'actina stimola la polimerizzazione dell'actina, facilitando potenzialmente l'attività fagocitica dei neutrofili dopo il pretrattamento con HBOT. Inoltre, l'HBOT promuove l'apoptosi nelle linee cellulari di linfociti T umani attraverso le vie mitocondriali, con un'accelerazione della morte linfocitaria post-HBOT. Il blocco della caspasi-9, senza influenzare la caspasi-8, ha dimostrato gli effetti immunomodulatori dell'HBOT.
Effetti sinergici dell'ossigenoterapia iperbarica con agenti antimicrobici
In ambito clinico, l'ossigenoterapia iperbarica (HBOT) viene spesso utilizzata in combinazione con gli antibiotici per combattere efficacemente le infezioni. Lo stato iperossico raggiunto durante l'HBOT può influenzare l'efficacia di alcuni agenti antibiotici. La ricerca suggerisce che specifici farmaci battericidi, come i β-lattamici, i fluorochinoloni e gli aminoglicosidi, non agiscono solo attraverso meccanismi intrinseci, ma dipendono anche in parte dal metabolismo aerobico dei batteri. Pertanto, la presenza di ossigeno e le caratteristiche metaboliche dei patogeni sono fattori cruciali nella valutazione degli effetti terapeutici degli antibiotici.
Numerose evidenze hanno dimostrato che bassi livelli di ossigeno possono aumentare la resistenza di Pseudomonas aeruginosa alla piperacillina/tazobactam e che un ambiente a basso contenuto di ossigeno contribuisce anche all'aumento della resistenza di Enterobacter cloacae all'azitromicina. Viceversa, alcune condizioni ipossiche possono aumentare la sensibilità batterica agli antibiotici tetraciclinici. L'ossigenoterapia iperbarica (HBOT) rappresenta un valido metodo terapeutico aggiuntivo, in quanto induce il metabolismo aerobico e riossigena i tessuti infetti e ipossici, aumentando di conseguenza la sensibilità dei patogeni agli antibiotici.
Negli studi preclinici, la combinazione di HBOT (ossigenoterapia iperbarica), somministrata due volte al giorno per 8 ore a 280 kPa, e tobramicina (20 mg/kg/giorno) ha ridotto significativamente la carica batterica nell'endocardite infettiva da Staphylococcus aureus. Ciò dimostra il potenziale dell'HBOT come trattamento adiuvante. Ulteriori indagini hanno rivelato che, a 37 °C e 3 ATA di pressione per 5 ore, l'HBOT ha notevolmente potenziato gli effetti dell'imipenem contro Pseudomonas aeruginosa infettante i macrofagi. Inoltre, la combinazione di HBOT e cefazolina si è dimostrata più efficace nel trattamento dell'osteomielite da Staphylococcus aureus in modelli animali rispetto alla sola cefazolina.
L'ossigenoterapia iperbarica (HBOT) aumenta significativamente anche l'azione battericida della ciprofloxacina contro i biofilm di Pseudomonas aeruginosa, in particolare dopo 90 minuti di esposizione. Questo potenziamento è attribuito alla formazione di specie reattive dell'ossigeno (ROS) endogene e mostra una maggiore sensibilità nei mutanti con difetti nella perossidasi.
Nei modelli di pleurite causata da Staphylococcus aureus meticillino-resistente (MRSA), l'effetto sinergico di vancomicina, teicoplanina e linezolid con HBOT ha mostrato un'efficacia significativamente maggiore contro l'MRSA. Il metronidazolo, un antibiotico ampiamente utilizzato nel trattamento di infezioni anaerobiche e polimicrobiche gravi come le infezioni del piede diabetico (DFI) e le infezioni del sito chirurgico (SSI), ha dimostrato una maggiore efficacia antimicrobica in condizioni anaerobiche. Sono necessari ulteriori studi per esplorare gli effetti antibatterici sinergici dell'HBOT in combinazione con il metronidazolo sia in vivo che in vitro.
L'efficacia antimicrobica dell'HBOT sui batteri resistenti
Con l'evoluzione e la diffusione di ceppi resistenti, gli antibiotici tradizionali spesso perdono la loro efficacia nel tempo. Inoltre, l'ossigenoterapia iperbarica (HBOT) potrebbe rivelarsi essenziale nel trattamento e nella prevenzione delle infezioni causate da patogeni multiresistenti, rappresentando una strategia fondamentale quando i trattamenti antibiotici falliscono. Numerosi studi hanno riportato i significativi effetti battericidi dell'HBOT su batteri resistenti clinicamente rilevanti. Ad esempio, una sessione di HBOT di 90 minuti a 2 ATM ha ridotto sostanzialmente la crescita di MRSA. Inoltre, in modelli di rapporto, l'HBOT ha potenziato gli effetti antibatterici di vari antibiotici contro le infezioni da MRSA. Alcuni studi hanno confermato che l'HBOT è efficace nel trattamento dell'osteomielite causata da Klebsiella pneumoniae produttrice di OXA-48 senza la necessità di antibiotici aggiuntivi.
In sintesi, la terapia con ossigeno iperbarico rappresenta un approccio multiforme al controllo delle infezioni, in grado di potenziare la risposta immunitaria e al contempo amplificare l'efficacia degli agenti antimicrobici esistenti. Grazie a un'accurata attività di ricerca e sviluppo, ha il potenziale per mitigare gli effetti della resistenza agli antibiotici, offrendo una speranza nella continua lotta contro le infezioni batteriche.
Data di pubblicazione: 28 febbraio 2025

